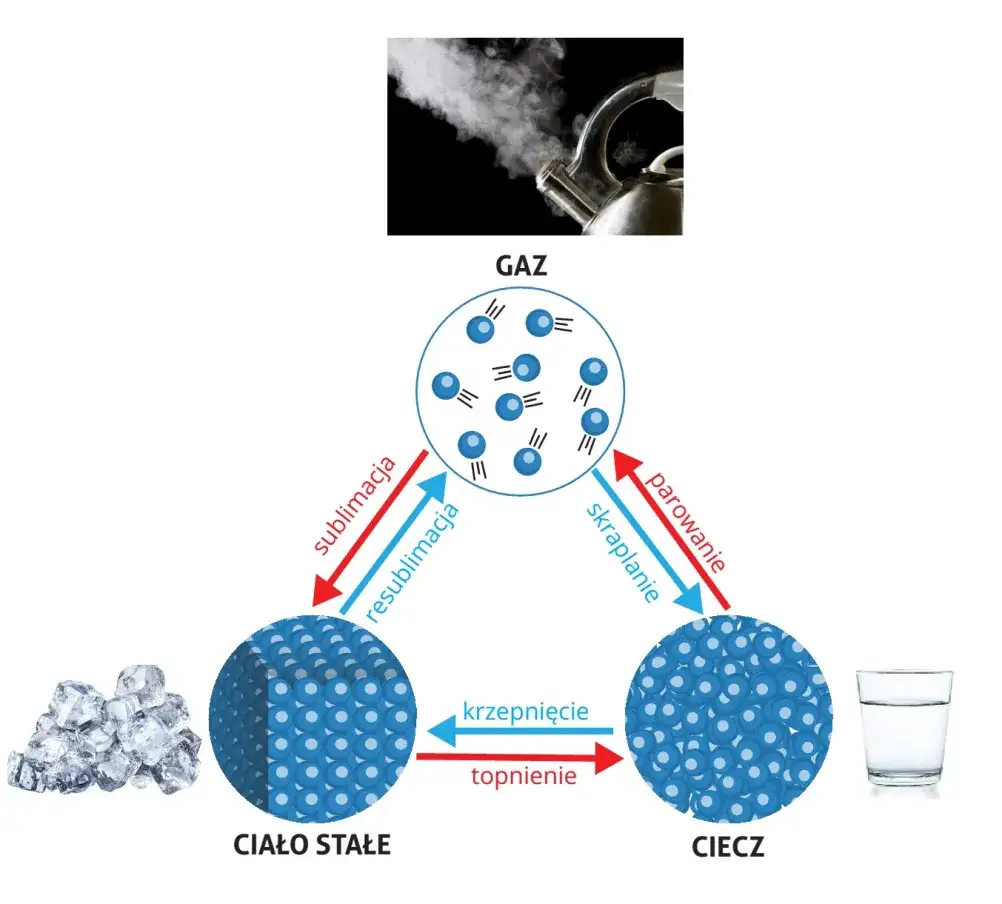
Woda to niezwykła substancja, która występuje w trzech podstawowych stanach skupienia: stałym (lód), ciekłym (woda) i gazowym (para wodna). Przejścia między tymi stanami nazywamy przemianami fazowymi. Zachodzą one na skutek zmian temperatury i ciśnienia. To fascynujące zjawisko ma ogromne znaczenie dla życia na Ziemi i wielu procesów przyrodniczych.
W zależności od warunków, woda może zmieniać swoją postać. Lód topi się w wodę, woda paruje w parę wodną, a para skrapla się z powrotem w wodę. Każda z tych przemian zachodzi w określonych warunkach temperaturowych i ciśnieniowych. Zrozumienie tych procesów jest kluczowe dla wielu dziedzin nauki i codziennego życia.
Najważniejsze informacje:- Woda występuje w trzech stanach skupienia: stałym, ciekłym i gazowym
- Przemiany fazowe to procesy zmiany stanu skupienia wody
- Temperatura i ciśnienie wpływają na stan skupienia wody
- Topnienie, krzepnięcie, parowanie, skraplanie, sublimacja i resublimacja to główne przemiany fazowe wody
- Diagram fazowy pokazuje, w jakich warunkach występują poszczególne stany skupienia wody
- Zrozumienie przemian fazowych wody jest ważne dla wielu dziedzin nauki i życia codziennego
Czym jest przejście fazowe wody?
Przejście fazowe wody to proces zmiany jej stanu skupienia. Zachodzi ono, gdy woda zmienia swoją formę z jednego stanu w drugi, na przykład z lodu w ciecz lub z cieczy w parę wodną.
Woda występuje w trzech podstawowych stanach skupienia: stałym (lód), ciekłym (woda) i gazowym (para wodna). Zmiany temperatury i ciśnienia są głównymi czynnikami powodującymi przejścia fazowe wody. Te warunki determinują, w jakim stanie skupienia znajdzie się H2O w danym momencie.
Charakterystyka stanu stałego i ciekłego wody
Właściwości lodu
Lód to stan stały wody, charakteryzujący się uporządkowaną strukturą krystaliczną. Cząsteczki wody w lodzie są ułożone w sześciokątną sieć, co nadaje mu charakterystyczną strukturę. Ta unikalna budowa sprawia, że lód ma mniejszą gęstość niż woda w stanie ciekłym. Woda zamarza w temperaturze 0°C przy normalnym ciśnieniu atmosferycznym.
Właściwości wody w stanie ciekłym
Woda w stanie ciekłym jest płynna i przyjmuje kształt naczynia, w którym się znajduje. Cząsteczki wody w tym stanie są w ciągłym ruchu, ale utrzymują się blisko siebie dzięki wiązaniom wodorowym. Woda pozostaje w stanie ciekłym w zakresie temperatur od 0°C do 100°C przy normalnym ciśnieniu atmosferycznym.
Proces topnienia - od lodu do wody
Topnienie lodu to fascynujący proces przemiany fazowej. Zachodzi ono, gdy temperatura lodu wzrasta powyżej 0°C, powodując rozluźnienie struktury krystalicznej. Do przeprowadzenia tego procesu potrzebna jest energia, zwana ciepłem topnienia.
Podczas topnienia, wiązania między cząsteczkami wody w lodzie słabną. To prowadzi do zmiany uporządkowanej struktury krystalicznej w bardziej chaotyczny układ charakterystyczny dla cieczy.
Krzepnięcie - jak woda zmienia się w lód?
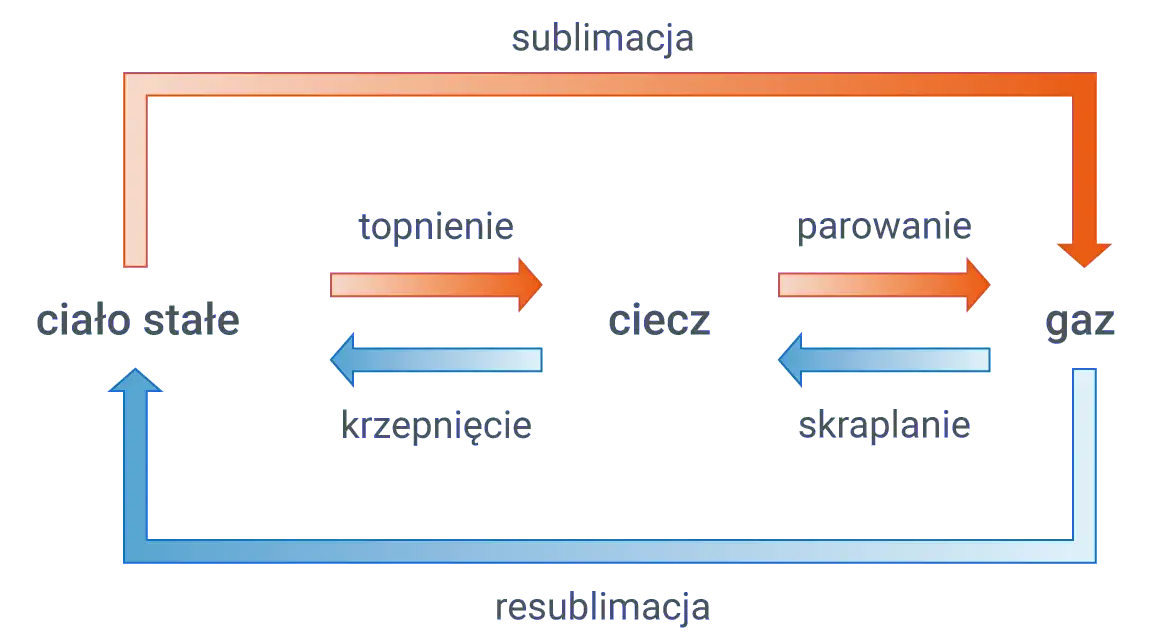
Krzepnięcie wody to proces odwrotny do topnienia. Zachodzi, gdy temperatura wody spada poniżej 0°C, powodując formowanie się struktury krystalicznej lodu. Podczas krzepnięcia woda uwalnia energię do otoczenia, co jest przeciwieństwem procesu topnienia.
Ciekawym zjawiskiem jest zwiększenie objętości wody podczas zamarzania. Lód zajmuje około 9% więcej przestrzeni niż ta sama masa wody w stanie ciekłym, co ma istotne konsekwencje w przyrodzie.
Kluczowa temperatura 0°C - punkt przejścia fazowego
Temperatura 0°C jest kluczowym punktem w przejściach fazowych wody. To granica między stanem stałym a ciekłym H2O. W temperaturze 0°C lód i woda mogą współistnieć w równowadze, co nazywamy punktem potrójnym.
- W temperaturze 0°C można obserwować jednoczesne topnienie i zamarzanie wody
- Ciśnienie atmosferyczne wpływa na dokładną temperaturę przejścia fazowego
- Zjawisko przechłodzenia pozwala wodzie pozostać w stanie ciekłym poniżej 0°C
Jak ciśnienie wpływa na przejście fazowe wody?
Ciśnienie ma znaczący wpływ na przejścia fazowe wody. Wzrost ciśnienia obniża temperaturę topnienia lodu i podnosi temperaturę wrzenia wody. To zjawisko ma ogromne znaczenie w przyrodzie, np. w formowaniu się lodowców czy gejzerów.
W wysokich górach, gdzie ciśnienie atmosferyczne jest niższe, woda wrze w niższej temperaturze. Z kolei pod dużym ciśnieniem, np. w głębinach oceanów, lód może istnieć w temperaturach wyższych niż 0°C.
| Ciśnienie (atm) | Temperatura topnienia lodu (°C) |
|---|---|
| 1 | 0 |
| 100 | -0,75 |
| 1000 | -7,5 |
Dlaczego lód pływa po wodzie?
Lód pływa po wodzie ze względu na różnicę gęstości. Gęstość lodu jest o około 9% mniejsza niż gęstość wody w stanie ciekłym. To zjawisko jest związane z unikalną właściwością wody, zwaną anomalią gęstości.
Woda osiąga maksymalną gęstość w temperaturze 4°C, a nie w punkcie zamarzania. Ta cecha ma ogromne znaczenie dla ekosystemów wodnych. Dzięki temu zjawisko, życie w zbiornikach wodnych może przetrwać zimę pod warstwą lodu.
Praktyczne zastosowania przejść fazowych wody
Przemiany fazowe H2O znajdują szerokie zastosowanie w przemyśle i technologii. Wykorzystuje się je w systemach chłodzenia, produkcji energii czy w procesach separacji. W geologii, cykle zamarzania i rozmrażania wody przyczyniają się do wietrzenia skał i formowania się charakterystycznych form krajobrazu.
W codziennym życiu stany skupienia wody odgrywają istotną rolę. Wykorzystujemy je w gotowaniu, konserwacji żywności czy w utrzymaniu higieny. Zrozumienie tych procesów pozwala nam efektywniej wykorzystywać wodę w różnych aspektach życia.
Fascynujące eksperymenty z przejściami fazowymi wody
Prosty eksperyment domowy może zobrazować przejście fazowe wody. Napełnij plastikową butelkę wodą do 3/4 objętości i umieść ją w zamrażarce. Po kilku godzinach zaobserwujesz, jak woda zamienia się w lód, zwiększając swoją objętość.
Ten eksperyment pokazuje, jak krzepnięcie wody wpływa na jej objętość. Demonstruje on, dlaczego zamarzająca woda może rozsadzić rury czy pęknięcia w skałach, co ma ogromne znaczenie w geologii i inżynierii.
Fascynująca podróż przez stany skupienia wody
Przejścia fazowe wody to niezwykłe zjawisko, które kształtuje nasz świat na wielu poziomach. Od mikroskopijnych przemian w strukturze cząsteczek po globalne zmiany klimatyczne, przemiany fazowe H2O odgrywają kluczową rolę w przyrodzie i technologii.
Zrozumienie procesów takich jak topnienie lodu czy krzepnięcie wody pozwala nam lepiej pojąć otaczający nas świat. Anomalia gęstości wody, dzięki której lód unosi się na powierzchni, ma fundamentalne znaczenie dla życia w zbiornikach wodnych. Jednocześnie, wpływ ciśnienia na temperatury przejść fazowych tłumaczy wiele zjawisk geologicznych i atmosferycznych.
Praktyczne zastosowania stanów skupienia wody są wszechobecne w naszym codziennym życiu i przemyśle. Od systemów chłodzenia po formowanie krajobrazu, woda w swoich różnych postaciach nieustannie kształtuje nasze otoczenie. Eksperymenty z przejściami fazowymi wody nie tylko fascynują, ale także uczą nas, jak ważne jest zrozumienie tych procesów dla rozwoju technologii i ochrony środowiska.